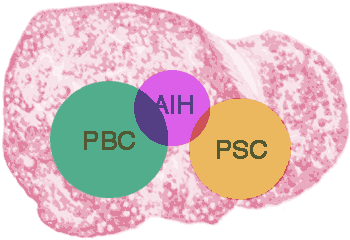
Die autoimmune Hepatitis (AIH), die primär biliäre Zirrhose (PBC) und die primär sklerosierende Cholangitis (PSC) werden zum Formenkreis der autoimmunen Lebererkrankungen gezählt. Bei diesen Lebererkrankungen spielen Immunreaktionen gegen wirtseigene Antigene eine herausragende pathogenetische Rolle. Lediglich für die AIH ist die verursachende autoimmune Reaktion hinreichend belegt, während für die anderen beiden Erkrankungen zwar Autoimmunphänomene beschrieben wurden, jedoch die Rolle weiterer konditionierender Faktoren und infektiöser Agenzien weiter zu klären sind.
Die AIH hat unbehandelt eine ungünstige Prognose und muss deshalb so früh wie möglich diagnostiziert und behandelt werden. Typischerweise finden sich verschiedene Autoantikörper (also Antikörper gegen körpereigene Strukturen), anhand derer verschiedene Untergruppen unterschieden werden können. Weiterhin werden verschiedene Immunreaktionen gegen Leberzellantigene beschrieben, welche die Immunpathogenese der Erkrankung zusätzlich belegen. Sehr wichtig scheint außerdem der genetische Hintergrund für die AIH zu sein, da diese bei Patienten mit bestimmten gewebespezifischen Antigenen auftritt.
Obwohl die feingeweblichen Veränderungen in der Leber nicht beweisend für eine AIH sind, gibt es einige charakteristische Veränderungen, die das Vorliegen einer AIH sehr wahrscheinlich machen. Therapeutisch hat sich die immunsuppresive Therapie mit Prednisolon und Azathioprin als sehr effizient erwiesen, so dass das Fortschreiten der akuten und chronischen Lebererkrankung bei den meisten Patienten aufgehalten werden kann. In den letzten Jahren wurden zudem sogenannte Overlap-Syndrome zwischen AIH und PBC bzw. seltener zur PSC beschrieben. Diese Veränderungen werden bei 15-20% der Patienten mit AIH bzw. PBC gefunden. Diese Patienten zeigen typische Gallengangsveränderungen und / oder antimitochondriale Antikörper (AMA) wie bei PBC und profitieren von einer kombinierten Therapie mit Prednisolon, Azathioprin sowie Ursodesoxycholsäure.
Die AIH wurde zuerst 1950 von Waldenström beschrieben und später von Kunkel et al. aufgegriffen. Die typischen klinischen Befunde sind Hepatomegalie und Splenomegalie (Vergrößerung von Leber und Milz) sowie uncharakteristische Beschwerden wie Abgeschlagenheit, Leistungsschwäche, Gelenkbescherden und Zeichen der chronischen Lebererkrankung wie Palmarerytheme und sog. Spider naevi ("Lebersternchen"). Häufig ist die AIH mit anderen Autoimmunerkrankungen assoziiert.
Differentialdiagnostisch sind weitere autoimmune Lebererkrankungen wie die PBC und PSC abzugrenzen, für die ebenfalls eine Autoimmunpathogenese angenommen wird. Beide Erkrankungen betreffen jedoch die intrahepatischen Gallenkanälchen bzw. die intra- und extrahepatischen Gallenwege und sprechen auf eine immunsuppressive Therapie im Gegensatz zur AIH meist nur ungenügend an.
Etwa 15-30 % der Patienten mit AIH bzw. PBC zeigen histologische Zeichen beider Erkrankungen sowie Auftreten von charakteristischen Autoantikörpern für beide chronische Lebererkrankungen. In der älteren Literatur wird hier oft von einer Autoimmuncholangitis gesprochen. Nach neueren Untersuchungen scheint es sich hier hauptsächlich um Patienten mit einer hepatischen Form der PBC zu handeln, die ebenfalls den charakteristischen immungenetischen Hintergrund AIH haben. Daher wurde für dieses Krankheitsbild der Begriff des Overlap- Syndroms geprägt . Overlap-Syndrome zwischen AIH und PSC wurden ebenfalls beschrieben, sind jedoch relativ selten.
Der Nachweis von verschiedenen Autoantikörpern ist für die AIH charakteristisch, jedoch ist es schwer, die Rolle der Antikörper in der Immunpathogenese zu verstehen, insbesondere da die Höhe der Antikörpertiter nicht mit der entzündlichen Aktivität zu korrelieren scheint. In verschiedenen Studien konnte insbesondere gezeigt werden, dass die Autoantikörper hauptsächlich gegen Leberzellmembranantigene und den humanen leberspezifischen Asialoglykoproteinrezeptor gerichtet waren.
Der histologische Nachweis einer Anreicherung besonders von T-Lymphozyten in den hepatischen Infiltrationen legt nahe, dass auch zelluläre Immunreaktionen an der Entstehung der Krankheit beteiligt sind.
Unverstanden ist jedoch, wie es anfänglich zur pathologischen Autoimmunreaktion kommt, da angenommen werden muss, dass die Autoimmunreaktionen durch das patienteneigene Immunsystem kontrolliert werden können. Die herausragende Rolle solcher autoreaktiven T-Lymphozyten für die Pathogenese der AIH wird weiterhin durch tierexperimentelle Modelle belegt.
In verschiedenen prospektiven Untersuchungen konnte die Wirksamkeit einer immunsuppressiven Therapie für die AIH belegt werden. Bewährt hat sich eine Induktionstherapie mit Prednisolon (1 mg/kg Körpergewicht per os täglich) in der Kombination mit Azathioprin (1-1,5 mg/kg Körpergewicht per os täglich) zur Erhaltung der Remission. Azathioprin hat einen Kortison einsparenden Effekt, so dass die anfänglich hohe Prednisolon- Dosierung schrittweise reduziert werden kann, meist bevor unerwünschte Nebenwirkungen auftreten. Das Therapieziel ist die rasche Normalisierung der Serumtransaminasen, was innerhalb der ersten Monate erreicht werden sollte.
Mit zeitlicher Verzögerung fallen auch die Gamma- Globulinspiegel langsam ab. Abhängig vom Therapieansprechen kann die Steroidgabe bei der überwiegenden Mehrzahl der Patienten auf 5 mg täglich reduziert werden bzw. ganz abgesetzt werden. Zu beachten ist jedoch, dass die Azathioprin-Therapie im Allgemeinen mit 50 mg täglich fortgeführt werden sollte, da nach einem kompletten Absetzen der immunsuppressiven Therapie bei ca. 80% der Patienten mit einer akuten Verschlimmerung und einer Reaktivierung innerhalb weniger Monate zu rechnen ist. Patienten, die nicht auf eine solche Prednisolon- Azathioprin-Kombinationstherapie ansprechen, können alternativ auch mit Cyclosporin A oder niedrigdosiertem Cyclophosphamid behandelt werden.
Ein besonderes Problem besteht für weibliche Patienten mit Kinderwunsch, da es während und nach der Schwangerschaft zu einer akuten Verschlimmerung der Erkrankung kommen kann und für das Azathioprin im Tierversuch schädigende Eigenschaften für den Embryo beschrieben wurden. Empfehlenswert ist hier, die Patientinnen mit der niedrigsten notwendigen Dosierung von Prednisolon und Azathioprin zu führen, da eine sichere Suppression der Krankheitsaktivität für die Sicherheit des Embryos sicher von größerer Bedeutung ist. Insbesondere nach erfolgter Entbindung ist mit einem schubweisen Verlauf der AIH zu rechnen, so dass diese Patientinnen sehr engmaschig kontrolliert werden sollten.
Die Prognose der AIH hängt vom Krankheitsstadium und entscheidend von einer ausreichenden Immunsuppression ab. Patienten ohne Leberzirrhose und therapiebedingtem Ruhen der Krankheit haben eine normale Lebenserwartung. Patienten mit kompensierter Zirrhose sind ebenfalls wenig beeinträchtigt , wohingegen die Prognose bei Patienten mit dekompensierter Leberzirrhose zum Diagnosezeitpunkt als ungewiss angesehen werden muss. Solche Patienten sind möglicherweise Kandidaten für eine Lebertransplantation.
In der Therapie der PBC hat sich die Ursodesoxycholsäure etabliert, welche vor allem zu einem besseren Gallefluss und damit zu einer Verminderung der Cholestase führt . Hierunter werden klinische Symptome der Cholestase, insbesondere Juckreiz (Pruritus) günstig beeinflusst. Hochdosierte Ursodesoxycholsäure (10-15 mg/kg Körpergewicht per os täglich) führt meist zu einer Reduktion der erhöhten Cholestaseparameter und der Bilirubinspiegel. Unklar ist jedoch die Beeinflussung der Gesamtprognose bei PBC.
Ausgehend von diesen Überlegungen sollten Patienten mit Overlap-Syndrom zwischen AIH und PBC kombiniert behandelt werden mit Prednisolon, welches schrittweise reduziert wird, und Azathioprin sowie mit Ursodesoxycholsäure in hoher Dosierung, obwohl hierzu bislang keine prospektiven Untersuchungen vorliegen. Eigene Erfahrungen zeigen, dass unter diesen therapeutischen Bemühungen die AIH-Komponente sehr gut in Remission zu bringen ist und anschließend lediglich die erhöhten Cholestaseparameter der PBC-Komponente zu beobachten sind.
Die nach Diagnosestellung früh einsetzende immunsuppressive Therapie mit Prednisolon in absteigender Dosierung in Kombination mit Azathioprin führt in den meisten Fällen der AIH zur klinisch vollständigen Remission und kann den Progress der Leberzirrhose verhindern. Selten kommen andere Immunsuppressiva wie Cyclosprin A oder Cyclophosphamid zum Einsatz. Patienten mit dekompensierter Leberzirrhose müssen eventuell durch die Lebertransplantation behandelt werden. Rezidive (Wiederaufflammen der Krankheit) danach sind sehr selten.
Das Overlap-Syndrom zwischen AIH und PBC wird symptomatisch mit hochdosierter Ursodesoxycholsäure sowie der o.a. immunsuppressiven Kombinationstherapie behandelt. Langzeitergebnisse aus prospektiv randomisierten Studien liegen bislang nicht vor.
Prof. Dr. Hans Löhr
Chefarzt Innere Abteilung
Johanniter Krankenhaus, Bonn
Lebertransplantierte Deutschland e.V.
Montag - Freitag 9:00 bis 13:00 Uhr
Telefon: 02302/1798991
Fax: 02302/1798992
Sie möchten Mitglied werden?
Hier gehts zur Beitrittserklärung
Sie möchten unsere Arbeit unterstützen?
Hier können Sie spenden